
2026年3月4日,中国医学科学院系统医学研究院/苏州系统医学研究所(以下简称“系统所”)李贵登团队与苏州大学医学院基础医学院吴华团队、苏州大学附属第一医院病理科郭凌川团队合作,在 Nature Metabolism 发表题为“Extracellular CD44 lactylation impairs CD8+ T cell function in KRAS-mutant colorectal cancer”的研究论文。该研究揭示结直肠癌细胞中KRAS突变通过重塑肿瘤代谢并增加乳酸分泌,进而通过诱导此前未被认知的胞外乳酸化修饰抑制T细胞介导的抗肿瘤免疫。

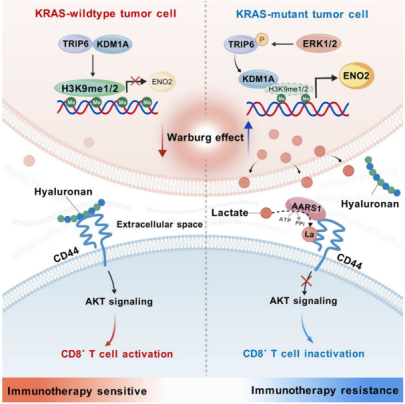
研究人员对临床结直肠癌样本进行定量蛋白组学分析发现,KRAS突变与TRIP6调控T细胞抗肿瘤免疫密切相关。机制解析发现,在KRAS野生型结直肠癌中,TRIP6通过与KDM1A结合,限制糖酵解酶ENO2的表达。而在KRAS突变型肿瘤中,异常激活的ERK1/2激酶促使TRIP6发生磷酸化,破坏其与KDM1A的结合,导致ENO2表达上调、糖酵解增强,乳酸在微环境中异常累积。有意思的是,结直肠癌细胞同时分泌乳酸转移酶AARS1。在细胞外基质中,肿瘤细胞分泌的乳酸可经AARS1介导,诱导CD8⁺ T细胞表面受体CD44在细胞膜外侧发生乳酸化修饰,从而抑制CD44与透明质酸的结合及其下游AKT通路激活,最终降低T细胞介导的抗肿瘤免疫。该发现首次证实细胞外乳酸化修饰的存在,打破了既往认为乳酸化修饰仅发生在细胞内的传统认知框架。
基于以上机制,研究团队进一步探索靶向治疗策略。研究者设计了包含TRIP6磷酸化位点的短肽PT6,可竞争性抑制结直肠癌细胞内TRIP6磷酸化。实验结果表明,PT6能够恢复KRAS突变结直肠癌细胞中TRIP6与KDM1A的结合,降低ENO2表达和乳酸产生,从而减少CD8⁺ T细胞表面分子CD44的乳酸化修饰并恢复CD8⁺ T细胞抗肿瘤活性。在动物体内,PT6治疗显著提升免疫检查点和CAR T过继疗法的免疫治疗效果。
综上,该研究揭示了结直肠癌细胞与T细胞间通过“KRAS突变—CD44乳酸化修饰”全新调控轴,将肿瘤代谢、胞外乳酸化修饰和T细胞抗肿瘤免疫紧密关联,为深入了解KRAS突变肿瘤的免疫治疗耐受机制提供了重要线索;同时,研究开发靶向TRIP6磷酸化的新型治疗策略有望为临床KRAS突变结直肠患者带来新型治疗方案。
系统所李贵登研究员与苏州大学医学院基础医学院吴华教授、苏州大学附属第一医院郭凌川教授为该论文的共同通讯作者。苏州大学医学院基础医学院博士生杨赟、郭欣,硕士生武文欣,苏州大学附属第二医院普外科吴勇主任和苏州大学附属第四医院病理科干文娟主任为该论文的共同第一作者。该研究得到国家自然科学基金、国家科技重大专项、江苏省自然科学基金以及中国医学科学院医学与健康科技创新工程、苏州市重点实验室等项目的支持。
原文链接:https://www.nature.com/articles/s42255-026-01482-3
供稿:系统院