
2026年3月13日,中国医学科学院基础医学研究所黄波团队在 Nature Chemical Biology 《自然-化学生物学》杂志发表题为“IDO1 regulating ROS rhythm reveals glycogenolysis/PPP as a cancer treatment target”(IDO 1调控活性氧节律揭示糖原分解-磷酸戊糖途径为癌症治疗靶点)的研究论文。该研究首次揭示经典免疫检查点分子吲哚胺2,3-双加氧酶1(Indoleamine 2,3-Dioxygenase 1,IDO1)是肿瘤细胞活性氧(Reactive Oxygen Species,ROS)节律变化的关键调控者。研究还进一步揭示人类肿瘤细胞针对乏氧所致的ROS节律破坏所建立的代偿机制,并提出IDO1与芳香烃受体(Aryl Hydrocarbon Receptor,AhR)双重抑制能够有效克服肿瘤细胞的治疗抵抗,为癌症治疗提供了全新的转化路径。
能量转化是细胞生命的本质,然而能量分子ATP生成必然伴随有害的活性氧(ROS)产生。ATP生成是细胞这枚硬币的一面,调控ROS由死向生则是硬币的另一面。此前学界已观察到肿瘤细胞胞内ROS以节律波(周期性振荡)的形式存在,然而形成这一底层现象背后的机制始终是一个谜。黄波团队通过HyPerRed荧光探针追踪发现,MCF-7等多种人类肿瘤细胞的ROS水平以约24小时为周期节律波动,而操控这一节律的核心分子却是一个酶分子IDO1。黄波团队发现,传统认为定位于细胞质的IDO1,实则存在核质穿梭行为:低ROS状态下,核内IDO1与Kelch样ECH相关蛋白1(Kelch-Like ECH-Associated Protein 1,KEAP1)结合,通过泛素-蛋白酶体途径被降解;当ROS水平升高时,IDO1借助核输出信号(Nuclear Export Signal,NES)与输出蛋白1(Exportin 1,XPO1)结合,转运至细胞质并与线粒体释放的血红素结合,形成具有酶活性的全酶结构。
IDO1全酶催化色氨酸生成Kyn,后者作为AhR的配体通过结合AhR发挥免疫抑制功能。黄波团队发现,Kyn直接与磷酸戊糖途径限速酶6-磷酸葡萄糖脱氢酶(G6P dehydrogenase, G6PD)结合。具体而言,Kyn结合G6PD的S278位点后,可降低底物G6P的米氏常数(Michaelis Constant,Km)并提升最大反应速率(Maximum Reaction Rate,Vmax),显著增强G6PD活性。这一别构效应能够迅速激活PPP通路,高效产生烟酰胺腺嘌呤二核苷酸磷酸(Nicotinamide Adenine Dinucleotide Phosphate,NADPH),而NADPH作为关键ROS清除分子,则及时降低胞内ROS水平,最终形成“IDO1-Kyn-G6PD-NADPH-ROS”的闭环调控,维持肿瘤细胞ROS节律波。
尽管肿瘤细胞内ROS以节律波的形式发生振动,但在某些情况下如乏氧,这种ROS节律波动会丧失,导致胞内ROS水平过高以及细胞死亡发生。然而,部分肿瘤细胞利用高ROS介导的AhR次磺酸化修饰,使得AhR能够结合到糖原复合体,促进糖原分解以及下游的磷酸戊糖途径,后者生成NADPH,快速清除ROS,并维持ROS在一个适度升高的水平,反而有助于肿瘤生长。这一发现完整解释了IDO1阻断剂的临床困境:单纯抑制IDO1尽管增强抗肿瘤免疫应答,但会导致ROS节律紊乱并激活AhR的代偿通路促进肿瘤,最终抵消其抗肿瘤效应。研究团队提出双重抑制策略:同时阻断IDO1与AhR,这一双重靶向策略同时靶向肿瘤免疫和肿瘤细胞活性氧,并堵死肿瘤细胞逃逸的通道,成为肿瘤治疗的新理念。
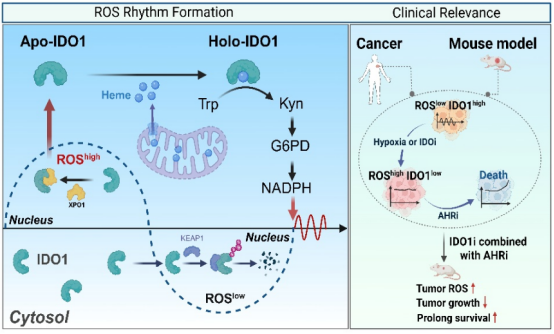
IDO1通过核浆穿梭调控糖原分解-磷酸戊糖途径维持ROS 节律示意图
该研究得到中国医学科学院医学与健康科技创新工程(2021-I2M-1-021;2023-I2M-2-005)、国家自然科学基金(82388201;82350111)及科技部重点研发计划(2022YFA1206000)等项目的资助。基础医学研究所黄波教授为论文通讯作者,课题组助理研究员周楠楠、博士生凌政、曹宪凯,以及中国医学科学院肿瘤医院主治医师张超奇为论文共同第一作者。
论文链接:https://www.nature.com/articles/s41589-026-02161-w
供稿:基础所