
2026年4月2日,中国医学科学院基础医学研究所黄波团队在 Nature Metabolism 《自然-代谢》发表了题为“Revitalizing p-GSK-3β via cysteine sulfenylation promotes hepatic insulin resistance by differentially regulating glycogenesis and gluconeogenesis”(通过半胱氨酸次磺酸化复活p-GSK-3β,通过差异性调控糖原合成与糖异生促进肝脏胰岛素抵抗)的论文。该研究发现活性氧(ROS)介导的GSK-3β特定位点修饰,是导致肝脏糖代谢紊乱的关键机制。
肝脏胰岛素抵抗(Hepatic Insulin Resistance, HIR)是2型糖尿病及多种代谢性疾病的核心病理基础,其恶性程度影响广泛,缺乏早期精准干预手段。经典胰岛素信号通路激活AKT通过促进糖原合成和抑制糖异生,共同维持血糖稳态。黄波团队研究发现,在HIR发生早期,尽管上游胰岛素信号(IRS-PI3K-AKT)在表观上保持完整,肝脏却出现了糖原合成减少与糖异生异常升高的现象。这种代谢失调形成的病理特征,使得寻找独立于经典通路之外的调控机制成为肥胖及糖尿病防治的理想策略。阻断GSK-3β的异常复活,恢复其原本受抑的失活状态,对代谢性疾病治疗而言,格外有意义。
针对肝脏糖代谢,胰岛素信号能够促进糖原合成并抑制糖异生,而氧化应激则诱发胰岛素抵抗。黄波团队发现,高脂饮食诱导的活性氧(ROS)作为核心触发信号,可诱导p-GSK-3β第178位半胱氨酸(Cys178)位点发生次磺酸化修饰。这种修饰后的p-GSK-3β能够突破磷酸化的失活限制而被重新激活,进而磷酸化糖原合酶GYS2并抑制其活性,阻碍糖原生成。同时,这种被“复活”的激酶还通过磷酸化转录因子FoxO1,解除其受到的抑制并促进其从胞浆移位至细胞核。FoxO1的这种核转位,需要ROS信号对GSK-3β活性的精准重塑。激活后的FoxO1上调糖异生关键酶基因的转录,为内源性葡萄糖的持续产生提供分子支撑,确保了肝脏在胰岛素存在的条件下仍维持高水平的糖输出。
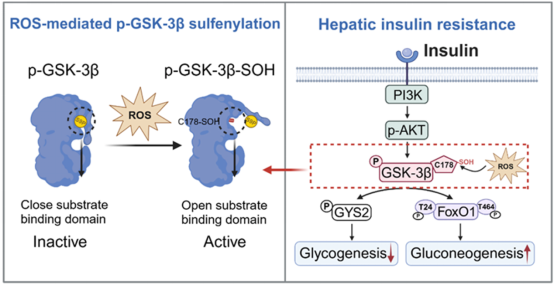 ROS诱导p-GSK3B再活化促进肝脏胰岛素示意图
ROS诱导p-GSK3B再活化促进肝脏胰岛素示意图
不同于以往主要关注晚期炎症信号JNK的研究,GSK-3β信号从HIR早期直至2型糖尿病发生发展全过程,始终对血糖稳态发挥关键调控作用。进一步研究表明,这种次磺酸化修饰具有明显的磷酸化依赖性,能够精准靶向已磷酸化的GSK-3β,从而既解释了上游信号完整而下游应答异常的“失配”现象,也揭示了代谢紊乱的关键触发机制。
更为重要的是,该机制已在原代细胞、动物模型及人源肝脏类器官等多层级体系中得到一致验证。这意味着,靶向GSK-3β次磺酸化位点的干预策略,有望选择性修复受损的肝脏代谢功能,凸显出该通路在代谢性疾病治疗中的潜在价值与精准调控优势。
研究工作得到中国医学科学院医学与健康科技创新工程(2024-12M-ZD-006,2021-12M-1-021,2025-I2M-XHXX-063,2025-I2M-KJ-008)等项目的资助,以及重大疾病共性机制研究全国重点实验室的支持。基础医学研究所黄波教授为论文通讯作者,课题组助理研究员陈洁、博士后刘卓航、博士生姜懿珅、江苏省人民医院副主任医师古鉴为论文共同第一作者。
论文链接:https://www.nature.com/articles/s42255-026-01507-x
供稿:基础所 专项处